今日头条
靖因长效小核酸新药国内获批IND。靖因药业新型siRNA疗法SRSD107注射液获国家药监局临床试验默示许可,拟开发用于预防或治疗动静脉血栓。SRSD107可通过特异性肝靶向凝血因子XI(FXI)mRNA,抑制FXI的蛋白表达,阻断内源性凝血途径的激活,从而达到抗凝血/抗血栓的作用。目前,该新药正在澳大利亚开展Ⅰ期临床试验。
国内药讯
1.华奥泰银屑病长效单抗启动Ⅲ期临床。华博生物和华奥泰生物开发的IL-17A单抗HB0017登记启动一项Ⅲ期临床,拟评估用于治疗中重度斑块状银屑病的疗效和安全性。该项研究由北京大学人民医院张建中博士牵头开展。在Ⅰ期临床中,HB0017(300mg)治疗患者皮肤症状清除(PASI 90)评分均达到100%;药物耐受性良好。此外,HB0017具有较长的半衰期,有望提供2~3月给药1次的维持期治疗方案。
2.科伦博泰ADC多项临床将亮相AACR。科伦博泰宣布其自主开发的TROP2 ADC新药SKB264(MK2870)将在AACR2024年会上公布用于治疗晚期胃癌经治患者以及治疗晚期非小细胞肺癌经治患者的两项Ⅱ期临床最新数据。值得一提的是,默沙东此次也将在会议上分享MK-2870针对既往治疗失败的EGFR突变或其他基因突变的非小细胞肺癌,以及联合Keytruda一线治疗PD-L1高表达非小细胞肺癌的临床进展。
3.强生克罗恩病单抗拟纳入优先审评。强生旗下古塞奇尤单抗注射液(guselkumab)获CDE拟纳入优先审评,用于治疗中重度活动性克罗恩病成人患者。此前,该新药这一适应症已被CDE纳入突破性治疗品种。Guselkumab(Tremfya)是全球首个获批的白介素23(IL-23)抑制剂,可靶向抑制IL-23这种在自身免疫性疾病中起到关键性作用的细胞因子。该新药已于2019年12月在中国获批治疗银屑病。
4.康弘1类抗肿瘤单抗获批临床。康弘药业旗下康弘生物1类生物制品KH801注射液获国家药监局临床许可,拟开发治疗晚期实体瘤。KH801能够与肿瘤细胞上的CD24特异性结合,通过阻断CD24/Siglec-10“别吃我”信号,提高肿瘤相关巨噬细胞(TAM)对肿瘤细胞的吞噬作用。在动物研究中,针对CD24的治疗策略对卵巢癌与三阴性乳腺癌具有治疗潜力,有望为这类难治性癌症提供新的解决方案。
5.AZ血癌ADC中国获批临床。阿斯利康靶向CD123抗体偶联药物(ADC)AZD9829获国家药监局临床许可,拟开发治疗CD123阳性恶性血液疾病。AZD9829能够将TOP1i载荷递送到表达CD123的癌细胞中,导致DNA损伤和细胞凋亡。目前,阿斯利康正在美国开展Ⅰ/Ⅱ期临床,评估AZD9829单独或联合治疗CD123阳性血液恶性肿瘤患者的安全性、耐受性、药代动力学和初步抗肿瘤活性。
6.星盛新辉“合成致死”小分子获批IND。星盛新辉小分子CHK1抑制剂XS-02胶囊获国家药监局临床试验默示许可,拟开发用于治疗晚期实体瘤。抑制CHK1会触发细胞周期阻滞,阻断肿瘤细胞的DNA损伤应答,达到“合成致死”的效果。公布于AACR2023年会上的临床前数据显示,XS-02在多种实体瘤模型(尤其是PARP抑制剂原发/继发耐药的肿瘤PDX模型)中,显示出良好的抗肿瘤能力,且安全性可控。
国际药讯
1.Formosa公司改良型眼科新药获批上市。Formosa公司和AimMax公司开发的0.05%丙酸氯倍他索(clobetasol propionate)眼科悬液APP13007获FDA批准上市,成为首个丙酸氯倍他索眼科产品,用于治疗眼科手术后的炎症和疼痛。在Ⅲ期临床中,APP13007治疗在清除炎症和缓解疼痛的疗效方面较安慰剂更优。远大医药拥有该新药在中国大陆、香港和澳门地区的独家开发和商业化授权。
2.司美格鲁肽慢性肾病III期临床积极。诺和诺德公布其GLP-1激动剂司美格鲁肽辅助治疗合并肾功能不全2型糖尿病和慢性肾病的Ⅲ期临床FLOW主要结果。数据显示,与安慰剂相比,司美格鲁肽使患者的肾脏疾病进展以及心血管和肾脏死亡风险降低24%,达到优效性终点。去年10月,由于司美格鲁肽的疗效达到预设标准,诺和诺德基于独立数据监查委员会(DMC)的建议提前终止FLOW试验。
3.罗氏/Alnylam长效降压药II期临床成功。罗氏与Alnylam开发的RNAi疗法Zilebesiran治疗轻中度高血压的II期KARDIA-2研究达到了主要终点。患者在标准治疗的基础上接受Zilebesiran(600mg,每6个月1次,皮下注射)治疗,3个月后,24h平均收缩压(SBP)较基线显著降低;且药物安全性良好。详细结果将在2024年美国心脏病学会年度科学会议上公布。
4.Empros公司口服减肥复方Ⅱ期临床积极。Empros Pharma公司口服组合配方EMP16(奥利司他/阿卡波糖)治疗肥胖或超重人群的Ⅱb期临床结果积极。数据显示,EMP16治疗使受试者平均体重减轻8%。该公司独有配方使两种化合物在胃肠道系统产生局部效果,增强疗效的同时降低潜在的副作用。Empros计划尽快开展两项用于治疗肥胖(伴或不伴有2型糖尿病)或超重人群的Ⅲ期临床。
5.Exonate公司FIC眼药水临床积极。Exonate公司基于SRPK1抑制剂开发的眼药水配方EXN407,在一线治疗轻中度非增生性糖尿病视网膜病和轻度糖尿病性黄斑水肿患者的Ⅰb/Ⅱa期临床中获积极结果。EXN407通过抑制SRPK1,可选择性地针对导致视网膜血管疾病进展的VEGF亚型,抑制眼内渗漏血管的异常生长。数据显示,与安慰剂相比,EXN407治疗能持续减少患者的黄斑厚度;有更多患者实现血管渗漏显著减少(60%vs20%)。此外,EXN407总体耐受性良好。
6.DMD基因疗法早期临床积极。REGENXBIO公司AAV8基因疗法RGX-202治疗4至11岁杜氏肌营养不良(DMD)患者的Ⅰ/Ⅱ期AFFINITY DUCHENNE试验结果积极。RGX-202旨在递送表达微肌营养不良蛋白的转基因进入骨骼肌和心肌组织。数据显示,接受RGX-202剂量水平2治疗的首例患者在三个月后,其微肌营养不良蛋白表达较标准对照提高75.7%,且在十周时观察到患者血清CK水平较基线降低77%,患者的力量与运动功能获得了初步改善。
医药热点
1.王卉晓履新安徽省中医药管理局党组书记。3月2日,据安徽省中医药管理局官网“局领导介绍”一栏信息显示,王卉晓已任安徽省卫生健康委员会党组成员、安徽省中医药管理局党组书记。公开信息显示,王卉晓,女,1967年11月出生,安徽合肥人,研究生学历,中共党员。她曾挂任安徽省合肥市庐阳区委常委、副区长;安徽省第二人民医院党委书记、安徽医学高等专科学校党委副书记等职。
2.北京积水潭医院成立日间手术中心。3月4日,北京积水潭医院日间手术中心正式挂牌,旨在有效减轻患者就医负担,推动医院高质量发展。日间手术中心计划开设床位15张,由手外科医师、麻醉医师、护理人员共同组成日间手术团队,试运行阶段主要收治手外科患者,可完成手部腱鞘炎、腱鞘囊肿、异物取出及内固定装置取出等手外科常规手术。符合日间手术的患者可以在24小时内完成“入院、住院、出院”全流程诊疗。
3.湖北省这家医院成立睡眠医学中心。近日,随州市中心医院睡眠医学中心正式成立。该中心是集睡眠障碍预防、监测、诊断与治疗于一体,为患者解决各类睡眠问题的综合诊治中心。睡眠医学中心开放病床30张,设置于季梁院区心身医学科内,配备多导睡眠监测系统(PSG)、重复经颅磁刺激治疗仪、团体生物反馈治疗仪、失眠治疗仪、心理CT等先进设备,并设有睡眠监测室、心理测量室、物理治疗室、个体心理治疗及团体心理治疗室。
评审动态
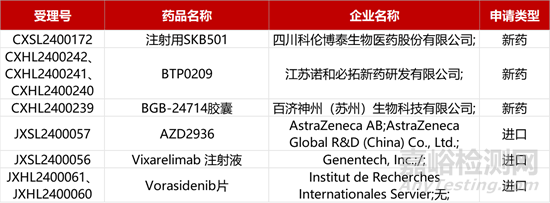
1. CDE新药受理情况(03月06)