【问】单抗产品上游共线生产的污染控制关注点是什么?
【答】上游共线生产的基本原则及流程: 《药品共线生产质量管理指南》已对药品研发、技术转移及生产阶段中生物制品的共线生产要求进行了详细的阐述,对于单抗上游的生产,企业在考虑共线生产时还应特别关注以下风险点:
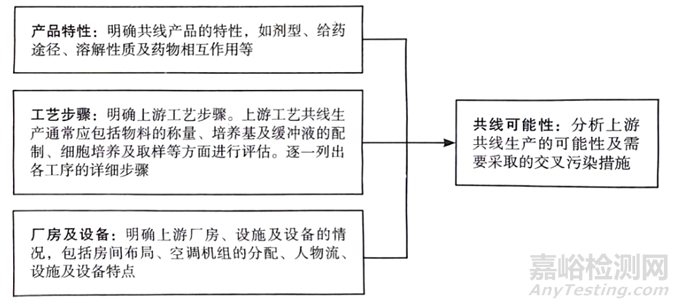
原则上,单克隆抗体不应与激素类生物制品、细胞毒类及高活性的药品共线生产。对于其他考虑共线生产的产品,需要经过充分的共线生产风险评估判断是否可以共线生产。典型的共线评估流程见下图。
上游共线评估流程图
上游共线生产的污染控制要求: 在单抗的共线生产过程中,相对于传统的不锈钢系统,一次性使用技术能更好地防止交叉污染,在充分确认系统密闭性的条件下,单抗多产品的共线应首先考虑使用一次性系统: 不锈钢系统用于单抗多产品共线生产时,需要更详细的风险评估和系统性的清洁验证来避免产品的交叉污染。
另外,GMP 中明确规定企业不得在同一生产操作间同时进行不同品种和规格药品的生产操作,除非没有发生混淆或交叉污染的可能。因此,单抗上游的共线生产中应考虑采用时间隔离 (错时生产) 的形式,或采取可靠的措施来支持同时生产 (如同一区域的独立密闭系统)。
·对于在生产过程中可能出现活性物质暴露的工艺步骤,在共线生产中考虑采用时间隔离 (错时生产) 的形式,如培养基配制、细胞接种等。错时生产的形式应建立生产线换产品管理的流程,确保在下一产品入场前完成清场及清洁,其操作应符合 GMP 的相关要求。作为密闭发酵阶段,可以同时进行产品的共线生产,但是仍然应该制定明确的管理流程来明确异常事件 (如泄漏) 的处理要求。
来源: 2023年药品GMP指南-无菌制剂下册P857-858