前言导读
创新医疗器械特别审查程序是为了保障医疗器械的安全、有效,鼓励医疗器械的研究与创新,促进医疗器械新技术的推广和应用,推动医疗器械产业发展,根据《医疗器械监督管理条例》《医疗器械注册管理办法》《体外诊断试剂注册管理办法》等法规和规章而制定的。
符合下列情形的医疗器械审查,适用于创新医疗器械特别审查程序:
(一)申请人通过其主导的技术创新活动,在中国依法拥有产品核心技术发明专利权,或者依法通过受让取得在中国发明专利权或其使用权,创新医疗器械特别审查申请时间距专利授权公告日不超过5年;或者核心技术发明专利的申请已由国务院专利行政部门公开,并由国家知识产权局专利检索咨询中心出具检索报告,报告载明产品核心技术方案具备新颖性和创造性。
(二)申请人已完成产品的前期研究并具有基本定型产品,研究过程真实和受控,研究数据完整和可溯源。
(三)产品主要工作原理或者作用机理为国内首创,产品性能或者安全性与同类产品比较有根本性改进,技术上处于国际领先水平,且具有显著的临床应用价值。
2023年7号创新医疗器械获公示
创新医疗器械特别审查申请审查结果公示(2023年第7号)
依据国家药品监督管理局《创新医疗器械特别审查程序》(国家药监局2018年第83号公告)要求,创新医疗器械审查办公室组织有关专家对创新医疗器械特别审查申请进行了审查,拟同意以下申请项目进入特别审查程序,现予以公示。
1.产品名称:前列腺癌磁共振图像辅助诊断软件
申 请 人:上海西门子医疗器械有限公司
2.产品名称:等离子皮肤治疗仪
申 请 人:合肥中科离子医学技术装备有限公司
3.产品名称:头颈动脉瘤CT血管造影图像辅助检测软件
申 请 人:上海联影智能医疗科技有限公司
4.产品名称:一次性使用冠状动脉旋磨装置
申 请 人:嘉兴匠鑫医疗科技有限公司
5.产品名称:介入式左心室辅助系统
申 请 人:安徽通灵仿生科技有限公司
6.产品名称:微创心肌旋切系统
申 请 人:武汉微新坦医疗科技有限公司
7.产品名称:一次性使用硅胶导尿管
申 请 人:泰州度博迈医疗器械有限公司
8.产品名称:腹主动脉覆膜支架系统
申 请 人:杭州唯强医疗科技有限公司
9.产品名称:多焦点人工晶状体
申 请 人:无锡蕾明视康科技有限公司
10.产品名称:多焦点人工晶状体
申 请 人:天津世纪康泰生物医学工程有限公司
11.产品名称:人DNA甲基化检测试剂盒(可逆末端终止测序法)
申 请 人:广州燃石医学检验所有限公司
相关产品与技术导读
笔者针对对11家企业相关涉及技术进行了详细解读,形成了个人学习笔记,本次重点关注的是杭州唯强医疗科技有限公司的腹主动脉覆膜支架系统,主要内容如下:(需要特别说明的是,上述创新医疗器械相关产品信息、专利技术仅仅作为笔者个人的学习笔记内容,为笔者学习过程的自行解读,并非与企业申报一致,相关内容以官方信息为准):
1、腹主动脉覆膜支架系统
申请人
杭州唯强医疗科技有限公司
公司简介
根据公司官网显示,杭州唯强医疗科技有限公司成立于2016年5月,落户于杭州国家高新技术产业开发区内,唯强医疗专注于外周血管介入医疗器械的研发、制造、销售和技术支持,主营产品为主动脉系列产品、静脉系列产品、下肢产品、导管和球囊等产品。公司目前已有多项产品取得NMPA注册证,另有多项产品在临床试验过程中,模块内嵌主动脉弓覆膜支架系统、胸主动脉支架系统两项产品通过创新医疗器械审批。公司注重医工合作、创新研发。
相关产品概览
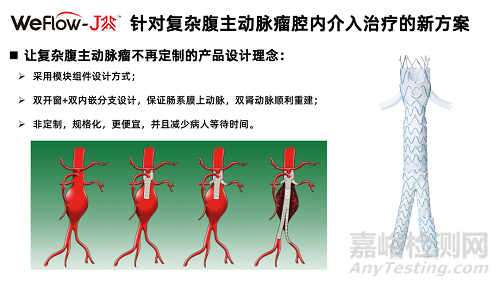
笔者认为进入创新通道的产品为杭州唯强医疗科技有限公司的WeFlow-JAAA腹主动脉覆膜支架系统。
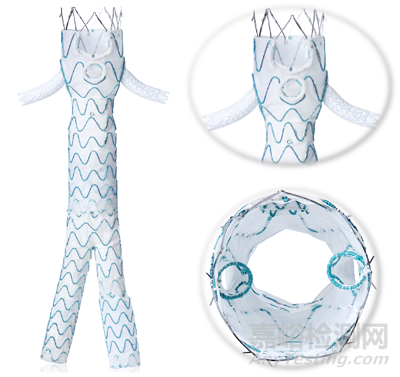
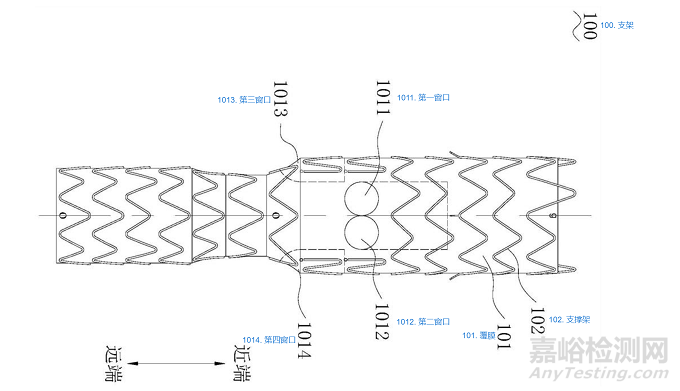
WeFlow-JAAA腹主动脉覆膜支架系统设计目的主要是治疗近肾腹主动脉瘤。其结构包括1个开槽、1个窗孔和2个内嵌分支分别用以CA、SMA、和RA的重建。开槽和开窗边缘有密封环设计用于防止内漏。该产品无需定制,可规格化生产。输送系统预置了3根导丝以快速建立分支动脉轨道。使用时主体经股动脉入路,到达预定位置半释放,由锁骨下动脉入路抓出预置导丝,重建SMA、CA和双侧RA,最后重建髂动脉。
WeFlow-JAAA系统是一款用于JAAA的新型腹主动脉非定制支架系统,由一个近端主体支架、一个远端双分支主体支架、髂支以及自膨式分支支架组成。设计的主要特定在于近端主体支架部分有两个标准的肾动脉内分支、一个短内嵌分支来加强肠系膜上动脉(SMA)的开窗以及腹腔干的U形结构。
WeFlow-JAAA系统
WeFlow-JAAA覆膜支架系统的设计:
•1个开槽+1个窗孔+2个内嵌分支;
•开槽可用于保留腹腔干动脉(CA);
•窗孔可单开窗重建肠系膜上动脉(SMA);
•近端主体直径:20-36mm;
•密封环设计用于提高密封效率,防止内漏;
•两个内嵌分支可用于重建直径为7mm、长度为15mm的肾动脉。
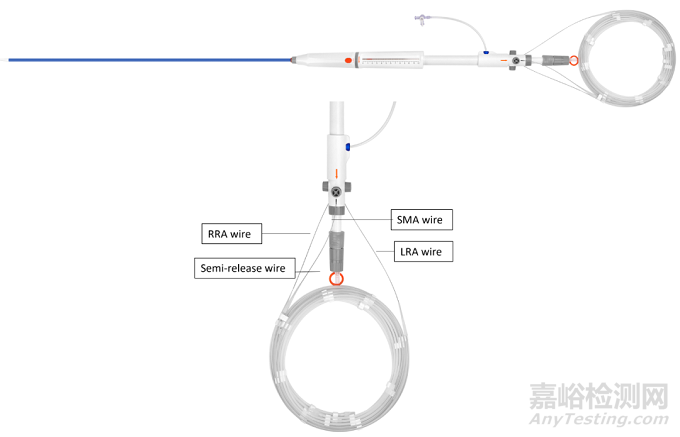
输送系统预置3根导丝,以快速建立分支动脉轨道。使用时,主体经股动脉入路,到达预定位置半释放,由锁骨下动脉入路抓出预置导丝,重建CA和双侧肾动脉,最后重建髂动脉。
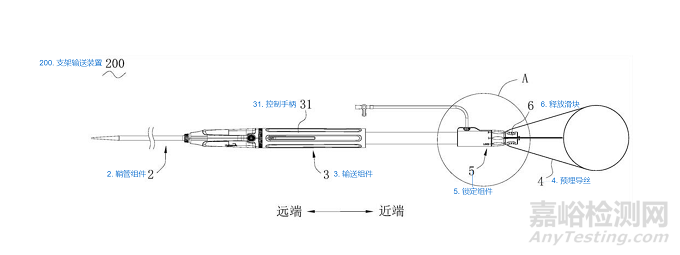
WeFlow-JAAA 输送系统
输送系统设计:
•尖端捕获释放和主体半释放使支架释放更可控;
•输送系统中预置了3根导丝可以快速建立分支动脉轨道,便于重建SMA和肾动脉。
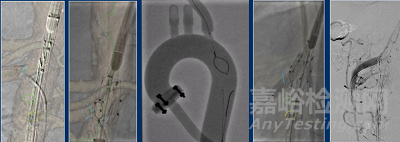
预埋导丝可在DSA下清晰显示
WeFlow-JAAA通过保留CA、单开窗重建SMA、内嵌分支重建双RA,为JAAA和部分肾旁AAA的腔内治疗提供了全新的解决方案。
专利技术解析
腹主动脉瘤(AAA)是一种常见的主动脉疾病,流行病学研究显示,AAA在男性中的发病率为5%,但在80岁及以上患者中,发病率增长到10%,而且其瘤体破裂的风险较其他人群更高。据预测,到2020年,我国80岁以上人口将达到3000万,90岁以上的将超过1200万,在未来将有越来越多的高龄AAA患者需要接受治疗。
现有治疗腹主动脉瘤的主要方式包括传统的开放手术及腹主动脉瘤腔内修复术,两种方式各有优势。腹主动脉腔内修复术(EVAR)自20世纪90年代报道首例被用于治疗腹主动脉瘤以来,因其创伤小、手术及住院时间短、术后恢复快、围手术期病死率及并发症发生率低等优点,在短短的20年内迅速发展。
腹主动脉瘤腔内修复术最大的优势在于不需要开胸开腹,无需钳夹阻断血管,术中无内脏器官缺血,并发症少。然而最大的限制是内脏大动脉不能被覆盖,尤其是肠系膜上动脉和肾动脉,涉及肾动脉领域的腹主动脉瘤腔内修复仍是难点。
目前,采用“开窗支架型血管”对这类病人实施支架型血管的植入治疗,即在腹主动脉植入主体支架,在主体支架开设开窗结构,在开窗结构再安装分支支架,通往分支血管。对腹主动脉瘤实施腔内治疗所植入的支架型血管涉及腹腔干动脉、肠系膜上动脉和左右肾动脉四条分支动脉血管的重建。
现有技术中主体支架植入动脉血管后,然后需要重复一遍植入分支支架,而在植入分支支架之前,需要引导分支导丝经由主体支架的开窗结构到分支血管中,然后通过分支导丝引导分支支架经由主体支架的开窗结构到达分支血管中,然而引导分支导丝到达分支血管非常困难,原因是分支导丝要穿过主体支架的开窗结构到达分支血管,分支导丝的远端对准并穿过主体支架的开窗结构非常困难,如何有效的减小分支导丝经由开窗结构到达分支血管的难度是当前医务人员和医疗研发人员必须共同解决的问题。
本发明提供了一种支架输送装置以及支架系统。该支架输送装置用于输送支架系统的支架。支架输送装置包括内设有输送通道的输送组件、穿设于输送通道的预埋导丝及设置输送组件近端的锁定组件;锁定组件包括由内而外依次设置的滑道件、固定件和操作件;滑道件与输送通道相通,滑道件的外周设有供预埋导丝穿出的过线部;固定件设有弹性悬伸的压紧臂,压紧臂与过线部相对;操作件活动地套设在固定件上并能够在锁定位置和解锁位置之间移动,操作件内部突设有按压部,按压部抵压或放开压紧臂,而使压紧臂压紧或释放预埋导丝。本发明通过预埋导丝方便引导分支导丝经支架上的窗口进入分支血管,锁定组件控制预埋导丝的锁定或释放,结构紧凑。
本发明至少具有如下优点和积极效果:本发明的支架输送装置中,通过输送组件上轴向贯通的输送通道可以连通至支架,而穿设在输送通道的预埋导丝即可以经支架上设置的窗口进入支架内侧,从而可以引导分支导丝经支架上的窗口到达分支血管,降低分支导丝到达分支血管的难度。预埋导丝通过锁定组件锁定或释放。其中,该锁定组件通过在操作件上设置按压部,利用操作件相对于固定件的活动改变按压部与压紧臂的相对位置,由此控制压紧臂的活动,从而能够将预埋导丝压紧于滑道件的走线部上或者将预埋导丝释放。锁定组件的构成简单,结构紧凑,操作方便。进一步地,利用按压部、压紧臂与走线部的配合对预埋导丝的压紧和释放进行控制,便于预埋导丝数量的扩展,即当预埋导丝具有多根时,适应性增加按压部、压紧臂与走线部的数量即可,而操作件、固定件和滑道件的主体结构无需改变,结构上占用空间小,整体结构紧凑,同时操作也更便捷。
知识拓展
腹主动脉瘤是指腹主动脉管壁永久性局限性扩张超过正常血管直径的1.5倍,是一种常见的动脉瘤。
腹主动脉覆膜支架治疗腹主动脉瘤的介入手段。腹主动脉瘤是腹主动脉的一段部位发生膨胀和扩张,若不及时治疗或手术切除,可能导致破裂、大出血、甚至死亡。腹主动脉覆膜支架经皮介入手段,通过导管插入体内,在瘤体内放置一个金属支架,将瘤体“堵住”,防止它进一步扩大或破裂。该技术具有创伤小、恢复快、手术风险低等优点,是目前治疗腹主动脉瘤的一种主要手段之一。
参考资料:国家药品监督管理局、唯强医疗、《门诊》杂志、血管资讯、医械知识产权等。