您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2020-09-10 10:39
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
「 本文共:15条资讯,阅读时长约:3分钟 」
今日头条
国内药讯
1.科伦「枸橼酸西地那非口崩片」国产首家申报上市。科伦药业枸橼酸西地那非口崩片上市申请获CDE受理。西地那非是一种PDE-5选择性抑制剂,枸橼酸西地那非口崩片为新剂型,同样用于治疗勃起功能障碍(ED)。目前国内已上市的西地那非产品有普通片剂和口腔崩解片,枸橼酸西地那非片生产厂家有辉瑞、白云山等7家企业。枸橼酸西地那非口腔崩解片获批企业仅有原研厂家辉瑞,科伦药业为国内首家提交仿制申请的企业。
2.再鼎尼拉帕利胶囊新适应症即将获批。再鼎医药「甲苯磺酸尼拉帕利胶囊」新适应症上市申请审评状态变更为「在审批」,预计即将获批,用于对含铂化疗完全或部分缓解的晚期上皮性卵巢癌、输卵管癌或原发性腹膜癌成人患者的一线维持治疗。尼拉帕利(则乐®)是再鼎医药从TESARO公司引进的一款口服PARP1/2抑制剂,已于2019年12月获NMPA批准,用于二线维持治疗。Insight数据库显示,尼拉帕利治疗小细胞肺癌、转移性前列腺癌均处于III期临床阶段。
3.复宏汉霖「贝伐珠单抗生物类似药」申报上市。复宏汉霖贝伐珠单抗注射液上市申请获CDE受理。这是国内第8款申报上市的贝伐珠单抗生物类似药。贝伐珠单抗原研是罗氏旗下安维汀,是全球首个可广泛用于多种肿瘤的抗血管生成药物。2019年安维汀全球销售额达到70.73亿瑞士法郎(约71.15亿美元)。该品种在2019年中国公立医疗机构终端销售额超过34亿元。目前该品种获批上市的企业有齐鲁制药和信达生物。
4.拜耳P2X3拮抗剂首次在华获批临床。拜耳1类新药BAY1817080获国家药监局临床试验默示许可,适应症为:治疗难治性和/或原因不明的慢性咳嗽(RUCC)。BAY1817080是一款P2X3拮抗剂,目前在全球处于Ⅱ期临床开发阶段。在一项Ⅰ/Ⅱa期临床中,与安慰剂相比,BAY 1817080显著减少患者24小时内咳嗽次数,而且耐受性良好。据ClinicalTrail信息,BAY 1817080至少有四项临床试验正在开展,涉及子宫内膜异位、咳嗽、膀胱过动症等适应症。
5.和誉CXCR4小分子抑制剂获批临床。和誉医药与X4 Pharmaceuticals合作开发的1类新药X4P-001(mavorixafor)获国家药监局临床试验默示许可,用于局部晚期或转移性三阴性乳腺癌。本次获批的临床研究可能为和誉与君实合作开展的mavorixafor与抗PD-1单抗特瑞普利单抗注射液联合用药临床试验。Mavorixafor是一款CXCR4拮抗剂,已在CXCR4基因突变引起的遗传性原发性自身免疫缺陷疾病WHIM综合征的II期临床中获积极结果,FDA已授予其孤儿药资格和突破性疗法资格。
国际药讯
1.9家新冠疫苗开发公司联名签署公开承诺。阿斯利康、BioNTech、葛兰素史克、强生、默沙东、Moderna、Novavax、辉瑞和赛诺菲9家公司的首席执行官共同签署了一项联合承诺,致力在推进首批新冠疫苗的全球监管申请和批准的过程中,维护科学过程的完整性。承诺明确,仅在通过符合监管机构(如FDA)要求的Ⅲ期临床试验,证明候选疫苗的安全性和有效性之后,才提交监管申请或紧急使用授权(EUA)申请。
2.默沙东Gefapixant治疗慢性咳嗽达Ⅲ期终点。默沙东在ERS 2020年会上公布其选择性P2X3受体拮抗剂gefapixant(MK-7264)用于治疗难治性或不明原因慢性咳嗽的两项关键性Ⅲ期临床(COUGH-1和COUGH-2)的积极结果。COUGH-1研究显示,与安慰剂相比,45mg gefapixant治疗组在12周时患者的24小时咳嗽频率减少18.45%(p=0.041);而COUGH-2研究显示,与安慰剂相比,45 mg gefapixant治疗组在24周时患者的24小时咳嗽频率减少14.64%(p=0.031)。两个研究中,gefapixant的安全性和耐受性与先前的研究报告一致。
3.鱼油成分药物Vascepa “护心”研究成果发表。Amarin公司鱼油成分药物Vascepa(icosapent ethyl)联合他汀类药物用于甘油三酯水平升高患者降低心血管疾病风险的EVAPORATE研究在ESC 2020年会和《欧洲心脏杂志》同步发表。结果表明,Vascepa联合他汀治疗将患者的低衰减斑块(LAP)体积显著减少了17%,而安慰剂组则增加了109%(P=0 .0061);其他类型动脉斑块的变化也在两组中表现出显著差异:总斑块体积变化:-9%vs11%(p=0.002)、总非钙化斑块变化:-19%vs0.9%(p=0.0005)、纤维脂肪斑块变化:-34%vs32%(p=0.0002)。不过,两组的甘油三酯变化没有显著差异,分别降低了89.3mg/dL和92.1mg/dL。
4.再生元/赛诺菲Dupixent治疗哮喘获长期疗效数据。再生元与赛诺菲联合开发的重磅IL-4/IL-13抑制剂Dupixent(dupilumab),在治疗中重度哮喘的Ⅲ期临床扩展试验中,疗效和安全性可维持长达3年,并且减缓患者的肺功能下降。具体为:与初始一秒用力呼气容积(FEV1)的基线水平相比,接受治疗96周时患者肺功能持续改善13-22%;治疗前患者的重度哮喘年发作率为2.09-2.17起,治疗后患者的重度哮喘年发作率为0.31-0.35起。
5.首创DPP1抑制剂brensocatib达II期临床终点。Insmed公司新型口服DPP1抑制剂brensocatib(INS1007)治疗非囊性纤维化支气管扩张症II期WILLOW研究的积极结果发表于《新英格兰医学杂志》上。与安慰剂相比,2种剂量(10mg和25mg)brensocatib显著延长了24周治疗期间发生首次肺部加重的时间(10mg组p=0.03;25mg组p=0.04);两个剂量组肺部加重风险分别降低了42%(p=0.03)和38%(p=0.046),肺部加重发生率分别降低36%(p=0.04)和25%(p=0.17);brensocatib的总体耐受性良好。Insmed公司计划下半年启动其III期临床。
6.AZ/牛津新冠疫苗一项Ⅲ期临床暂停。阿斯利康当地时间8日宣布,由于一名参加该公司与牛津大学合作研发的新冠疫苗试验接种的志愿者出现疾病,该公司将暂停正在进行的一项疫苗试验。英国BBC报道这一出现可能副作用的志愿者来自英国。阿斯利康并未透露相关细节,只是将这种可能的副作用称为“一种潜在的原因不明的疾病”。这是首个宣布暂停的已进入Ⅲ期临床试验的新冠候选疫苗。此前该疫苗正在英国、美国、巴西和南非进行Ⅲ期试验。
医药热点
1.瑞金专家团队完成升级版“最小起搏器”植入手术。9月5日,瑞金医院心内科主任吴立群教授团队,在海南省博鳌超级医院顺利完成MicraAV无导线双腔起搏器植入手术,这是该起搏器在大陆的首次临床应用。据介绍,此次植入的MicraAV是全球首个双腔无导线起搏器,体积仅有维生素胶囊大小,重量仅约2克,可以使用8-13年,兼容全身核磁共振扫描检查,患者感觉不到异物存在,是心脏健康的“隐形卫士”。
2.全球疫情之下跨国药企处方药销售14强。据日本医药行业分析师统计,今年上半年药品销售额达到100亿美元以上的有14家药企。处方药销售罗氏继续居于首位,诺华超越辉瑞跃居第二,主要因为辉瑞的重磅乐瑞卡受仿制药上市冲击,销售骤减10.2亿美元,下降至7.1亿美元。另外,百时美施贵宝因为完成对新基的并购,排名超越默沙东,上升至第5位,艾伯维排名保持不变,仍处于第7位。14家跨国药企中,仅有4家略有下滑。
3.世卫:中国抗疫行动有三方面特别突出。世卫组织多名高级官员7日给中国成功抗击新冠疫情并为世界抗疫提供有益经验点赞。世卫组织官员认为中国抗疫行动有三方面“特别突出”:首先是中国对公共卫生基础设施的巨大投入,从国家到省市再到社区,各个层面的公共卫生基础设施都发挥了重要作用;其次是中国人民的个人责任感,人们在不同场合都保持社交距离;第三是在病例数下行情况下仍持续提高疫情应对能力,人们认识到在一段时期内需要持续应对疫情。
股市资讯
【万孚生物】公司的核酸扩增分析系统获注册批准,其基于聚合酶链式反应(PCR)技术原理,与GN、GPC检测试剂配套使用,用于对人的血培养阳性样本中的病原菌及其耐药基因的定性检测。
【复星医药】子公司上海复宏汉霖生物制药的贝伐珠单抗注射液(HLX04)获药品注册审评受理,用于转移性结直肠癌及晚期、转移性或复发性非小细胞肺癌治疗。
【健康元】1)控股子公司丽珠医药的全资子公司(丽珠微球和丽珠制药厂)获得注射用醋酸奥曲肽微球的临床试验批准,用于下列肢端肥大症、功能性胃肠胰内分泌肿瘤相关症状的治疗;2)子公司海滨药业和上海方予收到盐酸左沙丁胺醇异丙托吸入溶液的临床试验批准,用于治疗气道阻塞性疾病有关的可逆性支气管痉挛。
审评动向
1. CDE最新受理情况(09月09日)

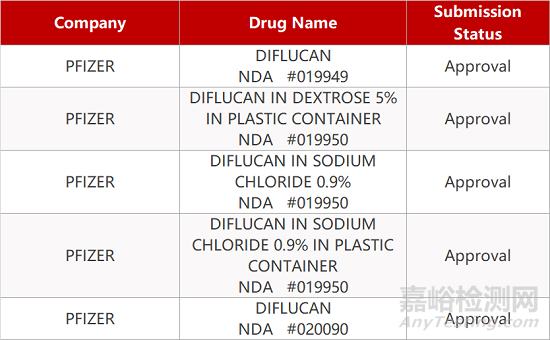
2. FDA最新获批情况(北美09月08日)
- The End -

来源:药研发


