您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-11-26 14:48
中药饮片制何首乌质量调查及监管建议
Investigation of Polygoni Multiflori Radix Praeparata Quality and Regulatory Suggestions
摘 要 / Abstract
目的:调查市场上制何首乌质量状况,提出监管建议。方法:从市场上抽取适量制何首乌中药饮片样品,按照《中国药典》2020年版一部“制何首乌”项下的规定对样品进行检验,并开展探索性项目研究,根据检验结果分析市场上制何首乌质量状况,提出相应监管对策。结果:共检验49批制何首乌,18批样品的游离蒽醌含量测定项不符合规定,不合格率为36.7%,其中13批样品涉嫌非法使用铁盐染色。结论:需进一步完善现行质量标准,建议增加铁元素限量的检查方法和限度规定。
Objective: To investigate the quality of Polygoni Multiflori Radix Praeparata in the market and put forward regulatory suggestions. Methods: Polygoni Multiflori Radix Praeparata samples were collected from the market, and tested according to the Chinese Pharmacopoeia. Then, exploratory research was conducted, and the general quality status of Polygoni Multiflori Radix Praeparata was summarized based on the testing and research results. Finally, relevant regulatory suggestions were proposed. Results: Of the 49 batches of samples tested, the content of free anthraquinone in 18 batches did not meet the requirements, reaching an unqualified rate of 36.7%. Among the 18 batches of unqualified samples, 13 batches were suspected of illegal use of iron salt staining. Conclusion: The current quality standards need to be further improved by adding testing method and specifications for iron limits.
关 键 词 / Key words
制何首乌;游离蒽醌含量;铁盐染色
Polygoni Multiflori Radix Praeparata; free anthraquinone content; iron salt staining
何首乌为蓼科植物何首乌 Polygonum multiflorum Thunb.的干燥块根,具有解毒、消痈、截疟、润肠通便的功效。制何首乌为何首乌的炮制加工品,具有补肝肾、益精血、乌须发、强筋骨、化浊降脂的功效[1]。制何首乌自《中国药典》1985年版开始收载,之后历版《中国药典》均有收载。《中国药典》2020年版中规定蒸至内外均呈棕褐色。何首乌经炮制后,外表的颜色随炮制时间的延长而加深,不同的炮制方法(炖法或蒸法)、炮制时间对游离蒽醌的含量影响较大。游离蒽醌的含量随着炮制时间的延长而增多。为保证成药的质量稳定,稳定的炮制方法及炮制时间是十分必要的[2]。
制何首乌主要含蒽醌类成份:大黄素、大黄酚、大黄素甲醚、大黄酚蒽酮等;二苯乙烯苷类成份:2,3,5,4'-四羟基二苯乙烯-2-O-β-D-葡萄糖苷、2''-O-单没食子酰基乙酯-2,3,5,4'-四羟基二苯乙烯-2-O-β-D-葡萄糖苷等[3]。
本文通过从市场上抽取适量制何首乌中药饮片样品,按照《中国药典》2020年版一部“制何首乌”项下的规定进行检验,根据检验结果分析市场上制何首乌质量状况,探究产生问题的内在原因,提出相应的监管对策。
01样品采集情况
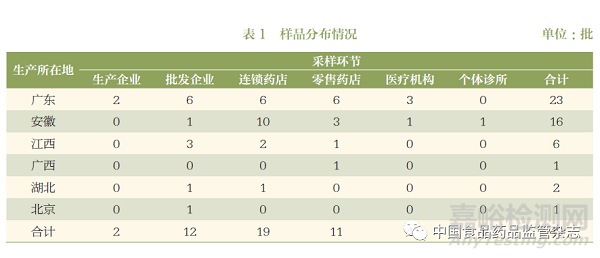
从生产、流通及使用环节采集制何首乌样品共49批,样品标识生产企业所在地涉及广东、安徽、江西、广西、湖北、北京6个省(自治区、直辖市),涉及生产企业共34家。样品分布情况详见表1。
02检验及结果分析
为更加全面调查制何首乌质量状况,对49批样品除按照《中国药典》2020年版一部“制何首乌”项下的规定进行检验外,还从铁盐筛查、电感耦合等离子体质谱(ICP-MS)法测定Fe的含量和安全性项目检验等三方面对样品质量进行探索性考察。
2.1 按照《中国药典》2020年版一部“制何首乌”项下进行检验
2.1.1检验项目和标准规定
《中国药典》2020年版一部“制何首乌”项下的检验项目包括性状、鉴别、检查(水分、总灰分)、浸出物及含量测定(二苯乙烯苷、游离蒽醌),各检验项目及标准规定详见表2。

2.1.2 检验结果及分析
性状:49批样品性状项目均符合规定,部分样品表面沉积一些黑褐色的粉末,部分样品的断面略呈角质样,淡棕褐色。
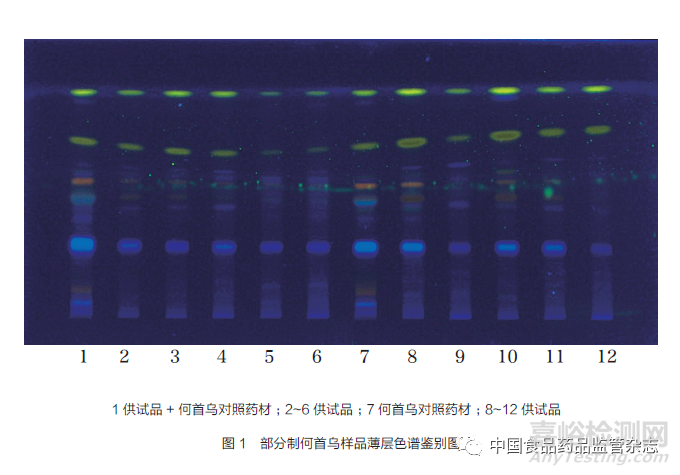
鉴别:49批样品供试品色谱中,在与何首乌对照药材色谱相应的位置上,显相同颜色的荧光斑点,均符合规定。部分制首乌样品薄层色谱鉴别图详见图1。
检查:49批样品的水分、总灰分结果均符合规定,其中水分检验结果为8.0%~11.8%,总灰分检验结果为2.1%~5.3%。
浸出物:49批样品的浸出物结果均符合规定,检验结果为6.6%~20.5%。
含量测定:49批样品中二苯乙烯苷的含量均符合规定,检验结果为0.79%~3.47%。49批样品中游离蒽醌的含量检验结果为0.02%~0.60%,其中31批合格、18批不合格,不合格样品检验结果为0.02%~0.07%。结合性状项目检验结果,不合格样品的断面均略呈角质样,淡棕褐色,提示可能存在炮制不规范的情况。
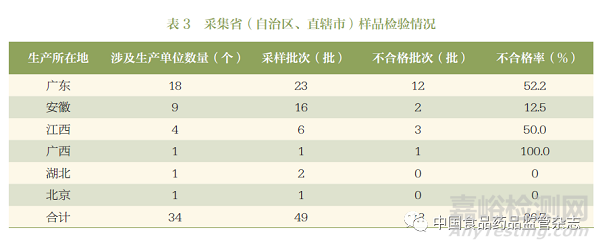
综上,按照《中国药典》2020年版一部“制何首乌”项下的规定对49批制何首乌样品进行检验,结果31批合格、18批不合格,不合格率为36.7%,不合格项目均为游离蒽醌含量测定。其中,产自广东的不合格批次最多,为12批,占不合格总批数的66.7%,占广东采样批数的52.2%。采集省(自治区、直辖市)样品检验情况详见表3。
2.2 探索性项目检验
制何首乌为何首乌的加工炮制品,炮制对其化学成份和药理作用均有一定的影响。何首乌中的蒽醌类成份遇Fe容易被氧化成为棕红色的蒽酮类成份,因此,何首乌炮制时要忌使用铁器。其外表的颜色随炮制时间的延长而加深,结合蒽醌类成份随着蒸制时间的延长而减少,水解反应后为游离蒽醌类成份,游离蒽醌的含量随着炮制时间的延长而增多,还原糖含量逐渐增多,其补益作用得到增强。
49批样品的外观差异可进一步细分为三类。第一类:表面黑褐色或棕褐色,断面角质样,棕褐色或黑色(图2)。第二类:表面棕褐色,断面略呈角质样,淡棕褐色(图3)。第三类:表面棕褐色,沉积一些黑色的粉末(图4)。18批游离蒽醌含量不合格的样品基本可归在第二类和第三类。



根据性状和游离蒽醌含量测定项目检验情况进行推断,部分生产企业加工何首乌时未按《中国药典》2020年版要求进行炮制,缩短炮制时间,以致制何首乌中游离蒽醌的含量低于标准规定。结合制何首乌非法染色的报道[4],为了更进一步探究18批不合格制何首乌样品是否存在以铁盐染色的方式制备出符合外观性状要求的制何首乌,本次探索性项目进行了铁盐筛查、ICP-MS法测定Fe的含量和安全性项目检验。
2.2.1 铁盐鉴别
取18批游离蒽醌含量不合格的制何首乌样品,参照《中国药典》2020年版四部通则“0301一般鉴别试验”中“铁盐”项下方法进行检验。结果除2批呈阴性反应外,6批呈阳性反应,提示样品在加工炮制时涉嫌使用了铁盐进行染色;10批呈不同程度的弱阳性反应,提示样品可能在加工炮制时或其生长环境受到不同程度的铁污染影响。
2.2.2 ICP-MS法测定Fe的含量
取18批游离蒽醌含量不合格的制何首乌样品,采用ICP-MS法进行测定。按全粉(样品粉碎,过四号筛)中Fe的含量来计,有4批样品检出较高含量的Fe,范围为551~1550μg/g,其余14批样品中Fe含量均低于500μg/g。按刮粉(刮取样品表面粉末)中Fe的含量来计,有13批样品中Fe含量均高于500μg/g,范围为553~12 575μg/g,刮粉与全粉中Fe的含量比值均大于3.5,认定13批样品中的Fe元素主要来源于样品的表面,提示这13批样品的生产炮制不规范,存在生产企业为使外观颜色符合《中国药典》2020年版要求,非法以铁盐进行染色。其余5批样品中Fe含量均低于500μg/g,刮粉与全粉中Fe的含量比值均小于3.5,提示这5批样品中的Fe含量可能受生长环境土壤的影响。
2.2.3 安全性项目检验
2.2.3.1 74种农药筛查
参照《中国药典》2020年版四部通则“2341 农药残留量测定法”中第四法农药多残留量测定法(质谱法),对49批样品进行74种农药筛查,其中有1批检出杀螟硫磷(残留量0.001mg/kg),《中国药典》2020年版“制何首乌”项下暂未对其农药残留限量进行规定,本次以GB 2763—2019食品安全国家标准《食品中农药最大残留限量》中“杀螟硫磷”项下茶叶规定的最大残留限量(不得过0.5mg/kg)作为参考限度,该批制何首乌的杀螟硫磷残留量远远低于参考限度,其余样品均未检出,即合格率为100%。
2.2.3.2 重金属及有害元素的残留量测定
参照《中国药典》2020年版四部通则“2321 铅、镉、砷、汞、铜测定法”,采用ICP-MS法对49批制何首乌中铅、镉、砷、汞、铜5种重金属及有害元素的残留量进行测定,参照《中国药典》2020年版一部黄芪的限度,结果49批样品的铅、镉、砷、汞、铜均未超过参考限度,合格率为100%。
2.2.3.3 黄曲霉毒素测定
参照《中国药典》2020年版四部通则“2351 真菌毒素测定法”中黄曲霉毒素测定法,结果49批样品均未检出黄曲霉毒素,合格率为100%。
2.2.3.4 二氧化硫残留量
参照《中国药典》2020年版四部通则“2331 二氧化硫残留量测定法”第一法酸碱滴定法和第二法气相色谱法,结果49批样品的二氧化硫残留量均小于150mg/kg[《中国药典》2020年版四部通则“0212 药材和饮片检定通则”规定药材及饮片(矿物类除外)的二氧化硫残留量不得过150mg/kg],合格率为100%。
03结 论
按照《中国药典》2020年版一部“制何首乌”项下的规定对49批制何首乌样品进行检验,18批样品的游离蒽醌含量测定项不符合规定,不合格率为36.7%。从铁盐筛查、ICP-MS法测定Fe的含量和安全性项目检验等三方面对49批制何首乌样品进行探索性考察,推断其中13批样品的生产企业可能存在炮制工艺不规范,以铁盐染色的方式制备出符合外观性状要求的制何首乌。
04讨论和建议
监管部门经过近年来的强力监管和精准打击,市场上制何首乌掺假行为得到基本控制,但部分生产企业为压低生产成本,不规范炮制饮片,使用铁盐染色等违法行为依然存在。生产企业应严格控制工艺参数,严格把关半成品及成品质量,规范炮制饮片。监督管理部门应加强对生产企业生产规范的监管力度,严厉打击非法染色等不规范炮制行为,从源头上控制不合格饮片流入市场。
现行质量标准未规定铁盐的限量标准,无法全面监控制何首乌的质量。建议在现行质量标准中加入铁元素限量的检查方法和限度规定,进一步完善质量标准。
美国食品药品监督管理局(FDA)在21CFR part 73中规定合成氧化铁可用于药品的着色,每天的摄入量不得超过5mg(以铁元素计)[5]。中国营养学会制定的我国居民膳食铁参考摄入量为男性成人15mg/d、女性成人20mg/d、老年人15mg/d[6]以及联合国FAO/WHO食品添加剂专家委员会(JECFA)规定的氧化铁每日容许摄入量(ADI)为0~0.5mg/kg[7],按60kg体重计算,每日摄入的高限为30mg[8]。按照《中国药典》2020年版规定的制何首乌用量6~12g,根据本次实验的测定结果,结合我国居民膳食铁参考摄入量15mg/d 的限定值及美国 FDA 拟定的每天不得超过5mg 的限量规定,建议将制何首乌中铁元素限度定为 0.5mg/g。按此限度,18批不合格样品中有4批制何首乌全粉中铁含量超过0.5mg/g,占22%;有13批刮粉中铁含量超过0.5mg/g,范围为0.553~12.575 mg/g,占72%。该结果的判定与铁盐鉴别以及ICP-MS法测定结果相吻合,初步判断可有效监控制何首乌使用铁盐染色的行为,但限度的合理性仍需进一步研究和验证。
引用本文
谢耀轩,张伟,肖丽和,康帅,王淑红*,马双成*.中药饮片制何首乌质量调查及监管建议[J].中国食品药品监管,2022(3):47-53.

来源:中国食品药品监管杂志


