您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2025-02-12 17:39
一、基本概况
1、自然环境
澳门是中国的特别行政区,位于中国东南部沿海,地处珠江口西岸。距香港60公里,距广州145公里。澳门处于国际时区的东八区,与北京没有时差。截至2024年6月底,土地面积33.3平方公里,海域面积85平方公里。
2、人口和行政区划
截至2023年底,澳门居住人口约68.4万人,人口密度为每平方公里约2.04万人。同时,居澳劳动人口约37.5万人,劳动力参与率为67.9%。按学历统计,具有高等教育学历的就业人口占44.9%,按年上升1.7个百分点。语言方面,行政机关、立法机关和司法机关除使用中文外,还使用葡文,葡文也是正式语言。粤语(广东话)为日常用语,英语在贸易、旅游和商业领域广泛应用。
澳门由澳门半岛、凼仔、路环岛组成,总面积33.3平方公里。
3、2024年出口概况
2024年1-10月,中国向澳门出口医疗器械总计约1.03亿元人民币,同比下降11.7%。
二、认证体系
1、监管机构和法规要求
澳门采用“进口许可”方式对医疗器械的进口进行监管,尚未建立医疗器械风险分类、注册认证审查及上市后监管体系;监管机构为澳门特别行政区政府药物监督管理局。
2、相关的“进口许可”政策
◆ 医疗器械 - 医疗卫材产品
第7/2003号法律 - 对外贸易法
第209/2021号行政长官批示 - 给予进口权限限的货物名单
◆ 体外诊断试剂 - 进口诊断及实验室试剂
第7/2003号法律 - 对外贸易法
第12/2022号法律 - 危险品监管法律制度
第27/2023号行政法规 - 危险品监管法律制度主要施行细则
第209/2021号行政长官批示 - 给予进口权限的货物名单
第107/2023号行政长官批示 - 制定危险品子分类和编码
三、“进口许可”申请
1、如何办理
①医疗卫材
◆ 办事指南:PS-1570 货物进口(药物监督管理局)- 进口医疗卫材产品的预先许可申请 - 澳门特别行政区政府入口
◆ 办理人:持有由经济及科技发展局发出”受管制外贸活动登记”的商号,即进口商。
◆ 办理流程及资料要求:确定产品分类→填写“预先许可”申请表、附上产品外包装样稿及说明书 → 递交“进口医疗卫材产品的预先许可申请”→预先许可申请通过→ 申请“产品进口准照”
* 备注:根据《第209/2021号行政长官批示 – 给予进口权限限的货物名单》法规提到已确定类别的医疗器械。
◆ 申请资料内容必须包括:产品名称、牌子(即商品名)、生产商名称、产品的有效成分及含量;如说明书或产品外包装用中、英、葡以外的文字写成,尚需提供中文或葡文的译文。
◆ 办理方式:现场办理及现场领取。
◆ 审批时间:3个工作天内签发货物进口预先许可证,进口预先许可证的有效期为签发日起计90天;即日签发产品进口准照,进口准照的有效期为签发日起计30天。
②进口诊断及实验室试剂
◆ 办事指南:PS-1570 货物进口(药物监督管理局) – 进口诊断及实验室试剂的预先许可申请 – 澳门特别行政区政府入口
◆ 办理人:持有由经济及科技发展局发出”受管制外贸活动登记”的商号,即进口商。
◆ 办理流程及资料要求:确定产品分类→填写“预先许可”申请表、产品资料或说明书 → 递交“进口医疗卫材产品的预先许可申请”→预先许可申请通过→ 申请“产品进口准照”
* 备注:根据《第209/2021号行政长官批示 – 给予进口权限限的货物名单》法规提到已确定类别的医疗器械。
◆ 申请资料内容必须包括:产品名称、成分含量、贮存条件及牌子(即商品名)等资料,以及尚需要的质量文件;注明有关产品将供给的使用者名称、其用途及用量;如产品含有第12/2022号法律所指的危险品,须同时于进口预先许可证的「产品名称」栏内标示产品的联合国编号或化学文摘社编号。
◆ 办理方式:现场办理及现场领取。
◆ 审批时间:3个工作天内签发货物进口预先许可证,进口预先许可证的有效期为签发日起计90天;即日签发产品进口准照,进口准照的有效期为签发日起计30天。
③产品分类申请
如不确定产品应按何种路径申请进口许可,须先申请产品分类。
◆ 办事指南
◆ 办理手续及所需文件:准备申请资料【产品包装、标签及说明书正本(如产品本身欠缺任何一项资料,申请人应注明及解释);其他文件,例如:产品全成分资料】 → 填写“产品分类申请书”, 如申请超过1种产品时,可递交已填妥的“产品分类申请书补充页”→ 递交申请 → 出具分类结果
* 备注:申请者所递交的资料必须与产品最终销售包装之所有内容及资料一致。
◆ 办理方式:现场办理及现场领取。
◆ 审批时间:18个工作天内发出分类结果的通知。
2、许可周期及费用
◆ 许可周期
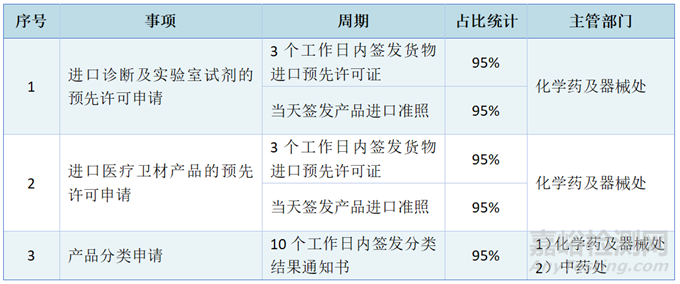
◆ 许可费用:免费

来源:广东医疗器械学会


