您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-04-29 11:38
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
必贝特HSP90抑制剂获批银屑病临床。必贝特医药1类新药BEBT-305片获临床试验默示许可,拟用于治疗中重度斑块型银屑病患者。BEBT-305(RGRN-305、CUDC-305)属于第二代HSP90抑制剂。它是一种Chaperone蛋白抑制剂,通过下调或降解参与自身免疫和炎症相关的多种细胞因子,抑制T-细胞参与的自身免疫和炎症反应。此次为该新药首次在国内获批临床。
国内药讯
1.百济神州PD-1食管鳞癌国际III期临床成功。百济神州PD-1单抗替雷利珠单抗(百泽安®)一线治疗食管鳞状细胞癌(ESCC)的全球Ⅲ期临床RATIONALE306结果积极。期中分析显示,替雷利珠单抗联合化疗显著改善患者的总生存期(OS),达到主要终点指标,而且联合治疗的安全性和耐受性特征与既往试验一致。目前,替雷利珠单抗已在国内获批8项适应症,该药用于上述适应症的上市申请正在审评审批中。
2.科伦Trop2-ADC启动Ⅲ期临床。科伦药业Trop2-ADC新药SKB264在Clinicaltrials.gov网站上登记启动一项用于治疗三阴乳腺癌的Ⅲ期临床试验。该项试验计划入组254例晚期复发性或转移性三阴乳腺癌患者,评估SKB264与标准疗法相比的治疗效果。目前,SKB264正在中美两国针对多个瘤种开展多项临床。在中国,同靶点药物已有8家申报;云顶新耀引进的Trodelvy、科伦药业的SKB264均处于Ⅲ期临床阶段。
3.绿竹重组带状疱疹疫苗进入II期临床。绿竹生物重组带状疱疹疫苗(CHO细胞,LZ901)登记启动一项II期临床,评价不同剂量的LZ901在50-70岁健康人群中接种的免疫原性和安全性。该项试验的主要研究者由湖北省疾病预防控制中心童叶青博士担任。LZ901通过肌肉注射后可主动地将VZV gE抗原呈递给机体的免疫系统,能增强机体的免疫系统产生体液免疫和细胞免疫的能力。
4.奥赛康Claudin18.2单抗胃癌早期临床积极。奥赛康生物Claudin18.2靶向单抗ASKB589注射液在I/II期临床研究中取得初步积极疗效。2例晚期胃癌患者在使用ASKB589治疗6周后,总体疗效评价结果均达到部分缓解,其中靶病灶明显缩小,部分非靶病灶消失,肿瘤标志物显著下降。在ASKB589联合CAPOX化疗方案一线治疗胃癌的剂量爬坡研究中,3mg/kg、6mg/kg剂量组中3例可评估患者分别在治疗6周和12周后达到部分缓解。
5.德琪合成致死ATR抑制剂报IND。德琪医药口服选择性ATR小分子抑制剂ATG-018已向澳大利亚人类研究伦理委员会(HREC)递交I期临床(ATRIUM研究)试验申请。该项临床旨在评估ATG-018单药治疗晚期实体瘤及血液肿瘤患者的安全性、耐受性和初步有效性,以及确定II期推荐剂量。ATG-018通过抑制ATR(共济失调性毛细血管扩张和Rad3-相关)激酶,来抑制肿瘤细胞的DNA损伤修复能力。该机制作用又被称为合成致死。
国际药讯
1.辉瑞口服CGRP受体抑制剂获批欧盟上市。欧盟委员会(EC)批准辉瑞和Biohaven合作开发的降钙素基因相关肽(CGRP)受体拮抗剂Vydura(rimegepant)上市,用于治疗急性、有或没有先兆的偏头痛,以及预防每月至少有4次发作的成人发作性偏头痛。这也是欧盟首款获批用于治疗和预防急性偏头痛的药物。在Ⅲ期临床中,与安慰剂相比,rimegepant显著减少患者每月偏头痛的天数;而且服用两小时内可减轻疼痛及改善偏头痛相关症状。
2.安进PCSK9类降脂药长期疗效积极。安进PCSK9抑制剂类降脂药Repatha(依洛尤单抗)治疗动脉粥样硬化性心血管疾病的Ⅲ期临床FOURIER两项OLE研究结果积极。患者接受Repatha治疗约5年,两项研究均未观察到新的长期安全性问题;随访期间,观察到低密度脂蛋白胆固醇(LDL-C)水平在医学上显著且持续降低,超过85%的患者LDL-C水平达到<40 mg/dL。
3.新一代CTLA-4单抗获FDA快速通道认定。OncoC4公司新一代CTLA-4单抗ONC-392获FDA授予快速通道认定,作为单药治疗先前接受抗PD-(L)1疗法后疾病进展的转移性非小细胞肺癌(NSCLC)患者。ONC-392能更有效地、选择性地清除肿瘤微环境中的调节性T细胞。与传统CTLA-4抗体不同,它不会引起CTLA-4的溶酶体降解,保留CTLA-4在身体其他部位的免疫耐受检查点功能。目前该药正在中美两国开展Ⅰ期临床研究。
4.VBL首创抗癌基因疗法获FDA快速通道资格。VBL Therapeutics首创腺病毒基因疗法ofra-vec (ofranergene obadenovec,VB-111)获FDA授予快速通道资格,联合紫杉醇治疗铂耐药卵巢癌。VB-111具有双重作用机制:抗血管生成/血管破坏和诱导肿瘤特异性免疫反应。此前公布的III期临床OVAL中期结果显示,在60例可评估患者中,CA-125蛋白水平得到缓解的患者,总缓解率(ORR)为53%,其中VB-111联合紫杉醇的ORR达到58%或更高。
5.卫材/渤健Aβ抗体最新研究积极。卫材与渤健开发的Aβ抗体Lecanemab在早期阿尔茨海默病(AD)患者中使用模拟建模获得的长期疗效结果发表在《Neurology and Therapy》上。结果显示,与标准治疗(SOC)相比,lecanemab+SOC组疾病进展为轻度、中度和重度AD的终生风险可能分别降低7%、13%和10%;lecanemab治疗组患者发展为轻度、中度和重度AD的平均时间分别延长2.51年(3.10vs5.61年)、3.13年(6.14vs9.27年)和2.34年(9.07vs11.41年)。
6.Sionna Therapeutics完成B轮融资。专注于囊性纤维化(CF)治疗领域的Sionna 公司宣布完成1.11亿美元的B轮融资。该公司正在开发的NBD1靶向小分子药物,旨在通过稳定囊性纤维化跨膜传导调节因子(CFTR)的NBD1蛋白域来完全恢复CF中缺陷的CFTR蛋白功能。Sionna计划在未来12个月内为其第一个NBD1靶向药物SION-638以及其针对ICL4的药物SION-109提交IND申请。
7.葛兰素史克2022Q1业绩增长32%。葛兰素史克公布2022年第一季度业绩报告,实现收入97.8亿英镑(130.56亿美元),同比增长32%。销售增长较高的药物分别有:新冠中和抗体Xevudy(13.07亿英镑);带状疱疹疫苗Shingrix(6.98亿英镑,+100%);三合一COPD/哮喘新药Trelegy(+57%),IL-5单抗Nucala(+22%)、系统性红斑狼疮药物Benlysta(+29%)。
医药热点
1.北京未出现不明原因儿童肝炎病例。北京市卫健委日前宣布,网传北京出现不明原因儿童肝炎病例为不实信息。北京市没有发生不明原因儿童肝炎病例及因此导致死亡的事件。针对近期国外报道的相关病例信息,为防患未然,最大程度保障首都地区儿童身体健康与生命安全,北京市卫健委下发《关于加强不明原因儿童肝炎病例救治的通知》,目的是提示相关医疗机构提高警觉,如出现病例要尽快查明原因、加强救治。
2.全国首家互联网职业病医院开诊。4月25日,广东省职业病防治院互联网医院正式揭牌开诊,为全国首家互联网职业病医院,将为职业病患者提供线上复诊、咨询、互联网诊疗等服务。据医院统计,开诊当天共接诊71人,答疑77条留言,涉及尘肺病、噪声聋、疑似职业病界定、职业禁忌证等相关判定,以及接触性鼻炎防治、尘肺病后期康复、上岗前职业检查、职业病申请表领取等问题。
3.上海12707名6岁以下儿童感染新冠。28日,上海市召开新冠疫情防控新闻发布会,介绍疫情防控最新情况。4月27日,上海市新增1292例新冠本土确诊病例和9330例本土无症状感染者,新增本土死亡病例47例,平均年龄84.7岁。据统计,本轮疫情上海累计报告6岁以下儿童阳性感染者12707例,约占感染者总数的2.4%,累计出院和解除集中医学观察人数7480例。主要收治在上海市公共卫生临床中心等定点医院,也有部分无症状的患儿在监护人陪同下,收治在方舱医院。
评审动态
1. CDE新药受理情况(04月28日)
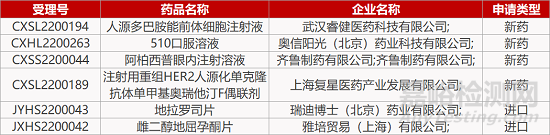
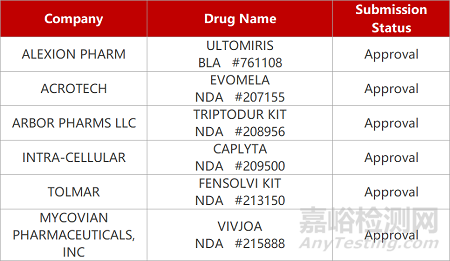

来源:药研发


