您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2022-01-19 20:58
导语:风险评估是提高无菌再处理质量的必要步骤,但是如何进行风险评估?如何解释风险评估的结果?这一课将有助于提供一些基本的指导。
Chasity Seymour
临床教育专家
学习目标
1、定义与风险评估相关的关键词
2、列出风险管理每个阶段执行的任务
3、制定无菌再处理的风险管理计划
风险评估有助于制定政策,实施必要的质量保证(QA)测试,并确保员工通过实践实现机构流程的最佳效果。尽管如此,很少有无菌处理(SP)标准、指南或推荐做法提供如何进行风险评估的细节,也很少有人解释如何处理结果。这一课将有助于提供一些基本的指导。
目标1、定义与风险评估相关的关键词
风险评估是有效风险管理计划的一部分。执行这些测试是为了识别实践中的失误或其他可能造成伤害的事件,然后帮助确定此类事件的可能性。风险管理系统通过降低风险评估期间发现的所有风险,努力消除潜在的危害。在进行风险评估过程之前,了解一些关键术语是很重要的。
伤害:伤害包括人身伤害、设备或设施损坏以及额外的金钱支出。与灭菌物品相关的危害包括患者感染、额外再处理增加的劳动力以及更换器械增加的成本。
不合格:不符合规定要求的结果。包括清洗后残留污染物的器械、不完整的器械套件和手推车延迟。
纠正措施:为消除已发现的不合格或其他不良情况的原因而采取的措施。这不应与改正相混淆。当装配小组发现一个污染的器械时,必须重新清洗。重新清洗必须立即进行(改正措施)。在调查过程中,小组发现了一把正在使用的损坏的旧刷子。制定刷子每次使用后的再处理政策,防止旧刷子在将来再次被使用;这是纠正措施。
预防措施:消除潜在不合格或其他不良潜在情况的原因的行动。预防措施的例子包括预防性维护、使用取用清单和定期水质测试。
风险:可能导致危害的不符合项的发生可能性。
概率:发生的可能性。
目标2、列出每个风险管理阶段需要执行的任务
风险管理是机构发现和管理风险的过程。
风险管理包括五个不同的阶段:
识别;
评估;
评定;
缓解;和监测
识别调查过程中可能造成危害的不符合项。任何不符合流程的操作都是不合格的。比如使用错误的灭菌周期、跳过清洗说明中的一个操作、无菌储存中的湿度水平超出规范要求。
有些流程简单,步骤少;有些流程复杂,步骤多,需要的设备、技术人员多。过程越复杂,就越容易出现不符合项。这就是为什么绘制流程图很重要。流程图显示执行的所有任务、执行每个操作的人、在何处进行传递和决策以及所需的所有工具和设备。开发流程图的团队应该包括完成工作的员工。对于流程图中需要的设备、供应品和仪表,审查制造商的书面使用说明(IFU)至关重要。永远不要想当然地认为,每次流程都是完全准确地遵循IFU的。
器械组灭菌
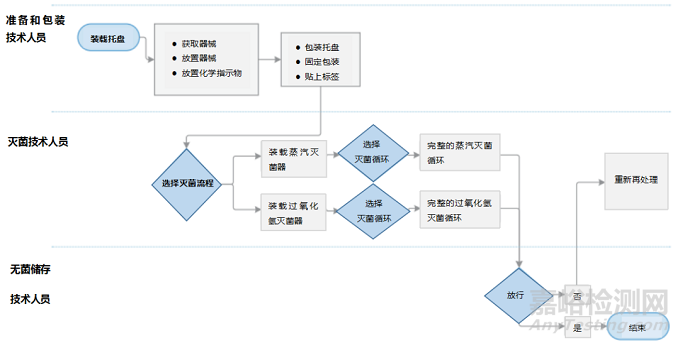
图1.流程图样例
危害识别可从列出潜在危害或发现潜在不符合项开始。列出潜在危害时,团队头脑风暴潜在的伤害。风险评估团队使用流程图来发现可能导致危害的不符合项。例如,一个危害是推迟手术。利用再处理流程图,团队可以识别出所有可能导致手术延期的错误。最好的办法是问:“为什么?”
一个“为什么”可以有很多答案。延迟可能是由于器械丢失、器械污染或化学指示剂失败等原因造成的。我们要探索每一种情况,并找出根本原因,直到完成一份全面的清单。
第二种风险评估方法从发现不符合项开始,确定所有可能的危害。鱼骨图是一种常用的方法;它着重于不合格情况的五个来源:材料、环境、过程、人员和设备。让我们看看图2中的一个例子。当旋臂堵塞时,污染物可能留在器械上。SP专业人员在装配过程中或在使用前在手术室(或)发现这些污染物。还有一种可能性是,直到手术中才发现器械污染。鱼骨图显示了这些事件的影响。如果在SPD中发现器械污染,则需要重新清洗。喷淋臂可能需要修理才能再次使用。重新清洗所需的额外处理时间可能会延迟器械回收到SPD,或者可能会延迟手术。重新清洗器械也可能增加成本。如果在手术室里发现了这个器械污染,则需要更换。此外,器械可能污染了器械台。两者都可能导致手术延期。
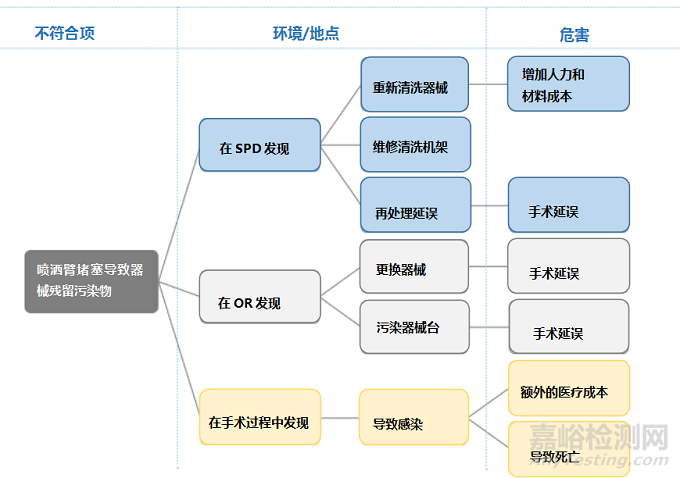
图2.关于器械残留污染物的鱼骨图
最坏的情况是污染没有被发现,导致外科感染。感染增加了病人和器械的成本。更糟糕的是,感染可能导致病人死亡。
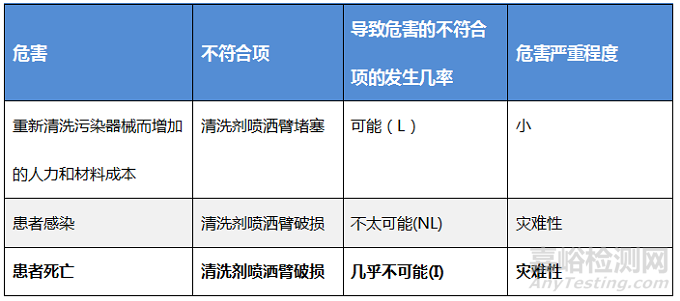
图3.风险评估样例
危害:手术延误
•为什么手术延期?外来器械迟到了。
•为什么外来器械会迟到?消毒供应中心太晚把托盘送到手术室。
•为什么SPD会延迟交付?外来器械供应商延迟向SPD交付器械托盘。
事件:外来器械供应商延迟交付托盘
在识别可能导致潜在危害的不符合项时,重要的是查看不符合项发现的所有区域,包括环境、水电、材料、设备、流程和人员。
一旦确定了所有危害和导致危害的事件,就到了评估风险的时候了。风险包括产生的危害和不合格事件发生的可能性。正如危害和发生概率不一样,所有的风险也不相等。SP装配员更容易找到污染器械,而不是工作人员。导致死亡的感染比需要治疗的感染发生的可能性更低。机构风险管理部门有分配风险值的政策和程序。在评估风险时,务必始终使用机构的严重性和概率评估规则。
一旦风险鉴定完成,就是时候评估风险了。评估时对风险进行排序,按发生的可能性和不可接受的影响排序。例如,机构可能会认为偶尔需要重新清洗器械是可以接受的。然而,病人死亡是不可接受的。再次,请参考机构的风险管理政策和程序。
通常情况下,风险矩阵是用来做决定的。风险矩阵将确定机构认为不可接受事件的概率和严重性。
风险矩阵
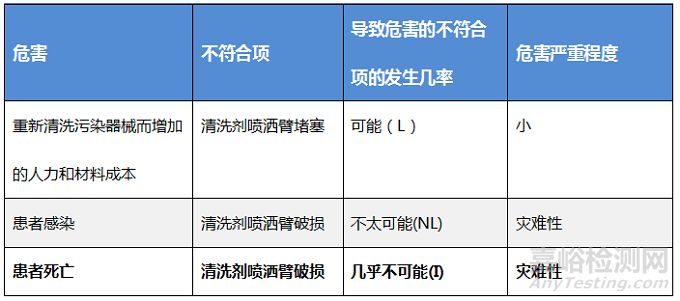
风险管理的目的是减少或消除风险。缓解是指为降低风险而采取的行动。风险的严重性无法改变。感染总是很严重,死亡总是灾难性的。降低风险的唯一方法是降低导致危害的不合格事件的发生可能性。
降低风险有三种方法。第一个也是最好的方法是完全消除风险。例如,消除可重复使用器械灭菌失败有关的风险的一种方法是使用无菌的一次性器械。然而,这是不可能的。通常,风险无法消除,但可以降低。
第二种方法是最小化发生的概率。采用预防措施、任务和测试来降低不合格事件发生的可能性。SPD使用许多技术来降低不合格事件发生的可能性。预防性维护、培训和能力测试、生物指示物测试、以自动化取代手工步骤以及器械检查都是将不合格事件发生可能性降至最低的方法。
降低风险并不意味着消除风险。风险预警是降低风险的最差的方法。程序、标牌和其他工具指出了技术人员的风险。在这三种工具中,这是最不有效的风险缓解方法。
风险管理中经常使用的工具是失败模式和影响分析(FMEA)。该工具将识别根本原因与分析风险控制结合起来。首先,识别失败模式;然后,列出了失败模式的影响。在此基础上,确定了当前的风险降低方法,并指定了风险等级。评估用于降低风险的任何新增任务、流程变更、材料或设备,并分配新的风险等级。始终记住,用于降低一个事件风险的任务可能会增加另一个事件的风险。
对于新的潜在风险,评估建议的风险缓解措施很重要。表1介绍了两项新的风险缓解活动:
(1)蛋白质检测试验和(2)管道镜检查。尽管这些减少了管腔中污染物材料的可能性,但是如果插入含有残留污染物的管腔后没有正确清洗,管道镜可能会带来交叉污染的新风险。这一风险将被列入清单并进行相应的评估。
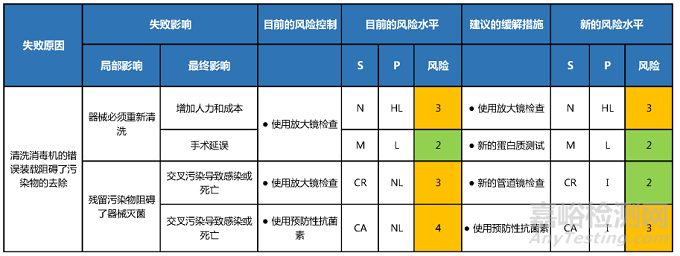
表1.失败模式效果分析表样例
风险管理的最后阶段是监测。监测风险缓解方法的有效性,并寻找可能在缓解过程中出现偏差的变化。监测也证实了关于概率的假设是正确的。评估取决于缓解措施。
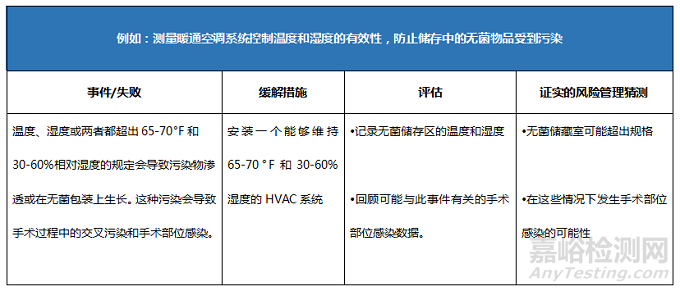
目标3、制定无菌再处理的风险管理计划
建立风险管理计划始于机构的风险管理政策和程序。首先,必须了解哪些部门必须参与,以及可能需要的报告流程和批准手续。
规划的第二步是确定项目的范围。无菌处理涉及广泛的部门、器械、再处理设备和材料。确定无菌再处理的部门很重要。这些部门就是客户。猜想客户的期望和需求是错误的。与客户会面、讨论和记录他们的需求以及SP提供的服务是至关重要的。这可以为客户提供现实的目标,为风险管理计划提供准确的信息。
接下来,选择从何处开始。无菌再处理部门(SPD)涉及一系列复杂的活动,无法在一天内进行评估。利用部门内物品的自然流动,或者一次只关注一个客户,根据合理性安排,而且要安排好工作量,以确保有足够的时间进入该区域。另外,确保有足够的时间对每个区域进行全面彻底的评估。
组建团队来处理流程的每个部分。确保包括机构的风险管理/预防、感染预防、生物医学技术人员、执行任务的SP技术人员、受影响部门的代表以及接收货物的客户。最终风险管理文件应以与评估类似的方式进行报告。一旦评估完成,缓解措施到位,培训完成,风险管理计划应按照机构程序进行审查和批准。
风险管理计划不是一成不变的;应定期审查计划和评估。在以下情况必须更新风险管理计划:在实施新流程、使用新器械或材料之前;当监测发现风险评估的估计概率和实时记录的概率之间存在差异时;发现以前未知的不合格情况时,或实施新的纠正措施时。
结论
风险评估不仅仅是指导文件页面上的文字。它是对过程、人员、环境、材料和设备进行的深思熟虑的审查,其目标是降低风险。这包括对机构的风险、技术人员的风险以及最重要的是对患者风险的评估。
参考文献:
ANSI/AAMI ST79:2017 Comprehensive guide to steam sterilization and sterility assurance in health care facilities
ANSI/AAMI ST90:2017 Processing of Healthcare Products – Quality ManagementSystems for Processing in Health Care Facilities
Guidebook for the Preparation of HACCPPlans. http://www.haccpalliance.org/sub/haccpmodels/guidebook.pdf

来源:鲁沃夫CSSD国际论坛


