您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2019-09-03 11:39
1.生物相容性测试及测试项目
生物相容性是指生物材料在机体特定部位产生各种复杂的生物、物理、化学的反应,即某些材料或者药物与人体接触或者植入体内是否能够“兼容”,会不会对我们的人体产生伤害。需要做生物相容性测试的产品一般是医疗器械以及医疗药物,生物相容性测试也称医疗器械生物学评价,对医疗器械产品进行有安全性和有效性评价是产品进入临床试验前的关键环节,同时也是产品上市后市场销售情况的关键所在。
生物相容性测试项目比较多,主要有细胞毒性、致敏、刺激、全身毒性(急性毒性)、亚慢性毒性(亚急性毒性)、遗传毒性、植入、慢性毒性、致癌性、生殖和发育毒性和生物降解等。不是所有的医疗器械产品都要做全套的测试项目,企业只需要根据自身产品的使用特点,结合与人体接触的部位和时间长短,查找符合自身产品的项目进行评价就可以了。实际上,对接触人体皮肤、粘膜和损伤表面等风险等级较低的医疗器械来说,需要进行试验的三个项目是:体外细胞毒性试验、皮肤致敏性试验、刺激试验,也称生物学评价的基础三项。当产品与人体长期接触或者接触部位风险较高的情况下,产品才需额外增加亚急/慢性毒性、遗传毒性、植入等试验。国标ISO10993-1:2018发布后,生物相容性测试参考项目发生了变化,具体测试项目见下表(红色:新增项目)。
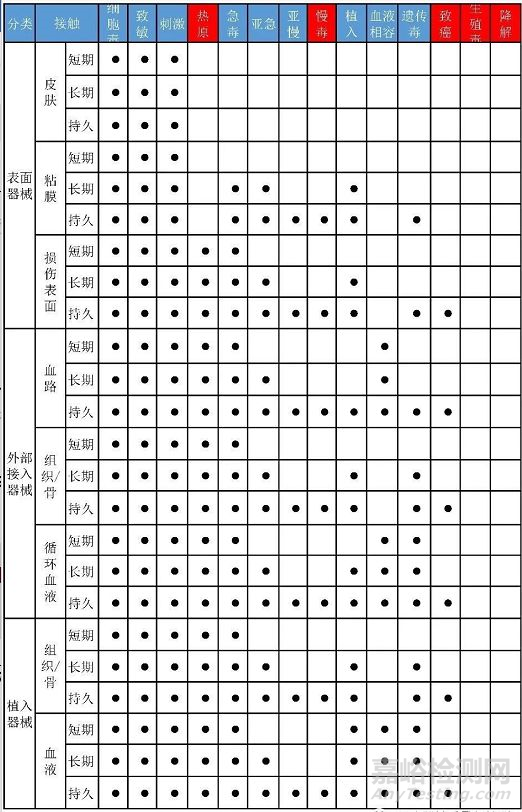
2.生物相容性测试标准及流程
目前生物相容性测试所参照的标准是ISO10993和GB/T16886,两种标准的内容基本一致,主要测试项目有以下几个部分:见下表。
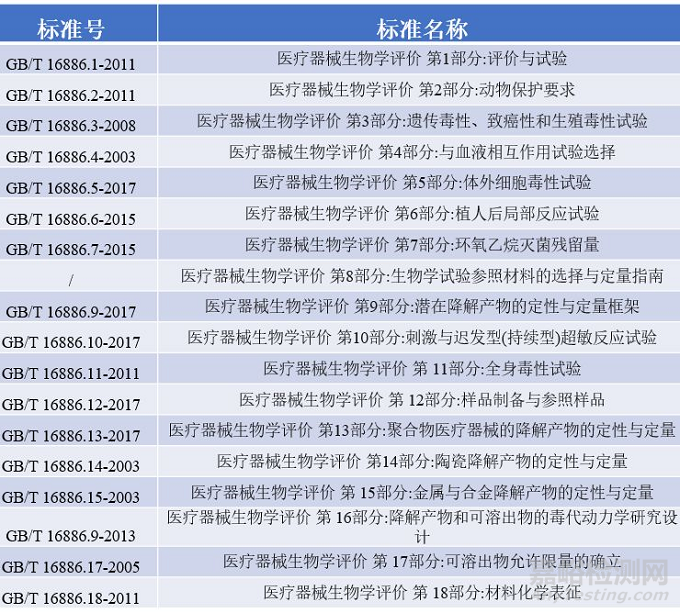
ISO10993和GB/T16886标准对具体的生物学评价过程进行了规定,在进行生物相容性试验之前需要鉴别材料成分,并做化学表征测试。体外诊断产品并不和人体直接接触,ISO10993和GB/T16886标准不适用于此类产品,其他与人体直接接触的有源医疗器械和无源医疗器械的安全性评价都需按照以下流程图进行测试。
医疗器械生物学评价流程图
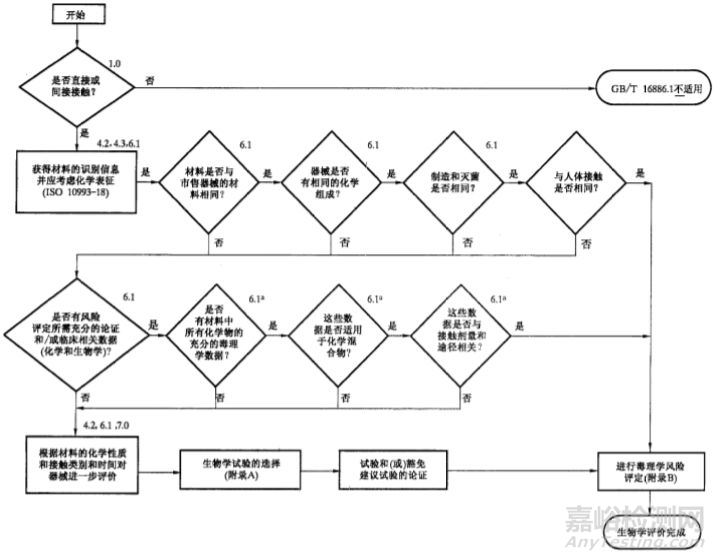
3.生物学评价试验的特点及评价原则
1)大部分体内、体外生物学试验检测样品在规定的浸提条件下浸提,进行试验。
2)直接用材料和医疗器械植入体内,与组织、血液或体表组织、血液接触进行试验,大部分的体内试验是通过外科无菌手术操作方式进行的。
3)进行体外细胞培养,观察样品的细胞毒性,测定浸提液或材料对细胞溶解(细胞死亡)、抑制生长的毒性作用。
4)致癌试验是用不同形状、大小、表面状态的材料植入体内某一部位,观察动物整个寿命期材料和医疗器械对体内潜在的致癌作用。
5)血液相容性试验是通过材料和医疗器械直接接触血液,首先观察对血小板激活、血栓形成的凝血作用,其次观察血浆蛋白、血液有形成分和补体系统、细胞因子的作用。
6)植入试验是将生物材料和医疗器械埋入动物体内某些部位,埋入不同时间材料对局部的组织病理学的改变。
7)降解试验是采用各种体内外方法,测定材料和医疗器械的降解程度、力学强度的变化,了解降解产物在体内的吸收、分布、代谢过程,评价材料对机体的有害作用。
生物相容性测试遵循的两大原则有生物安全性原则和生物功能性原则。生物安全性原则的目的在于消除生物材料对人体器官的破坏性,比如细胞毒性和致癌性。生物材料对于宿主是异物,在体内必定会产生某种应答或出现排异现象,因此要对生物材料进行生物安全性评价,确保材料被宿主接受,不产生有害作用。生物功能性原则是指在特殊应用中“能够激发宿主恰当地应答”的能力,不仅要对生物材料的毒副作用进行评价,还要进一步评价材料对生物功能的影响。
4.生物学评价发展趋势
传统的生物学评价主要内容和手段是在细胞和组织水平上,利用形态学的检测方法观察材料与机体短期和长期的相互作用,随着新型医疗器械和生物材料的迅速发展,器械或材料的组成形态、植入部位及用途日趋复杂,对器械或材料的评价相应提出了更高的要求,发展快速,特异,系统的评价体系至关重要。分子生物学先进检测手段的应用使生物学评价向细胞和分子水平迈进,发展体外实验,采用灵敏,特异,先进的检测手段,优化并减少实验动物数量,建立器械和材料对分子、细胞、机体相互作用的系统性评价是医疗器械和生物材料生物学评价的最终目的。

来源:Internet


