您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-03-29 09:29
引言
随着现代工业的快速发展,世界各国对能源的需求呈爆炸式地增长,随之而来的能源短缺和环境污染等问题逐渐严峻。在今后很长一段时间内,能源短缺问题将是世界能源可持续发展所面临的巨大挑战。随着储能技术的发展,锂离子电池、超级电容器、锂硫电池、钠硫电池以及液流电池等技术近年来成为关注的重点。相比其他基本处于试验阶段的储能技术,锂离子电池技术上比较成熟,已经实现了较大规模的商业化应用,几乎已经成为世界上应用最广泛的电池。
锂离子电池具有比能量高、自放电弱、循环性能好、无记忆效应和环保等优点,是目前最具发展前景的二次电池。锂离子电池主要由正负极和电解质组成,对于负极材料,金属锂负极在上世纪七十年代首先得到应用,随后是合金材料[1]。由于其较差的安全性能,锂电池在市场中的推进遭遇巨大挫折。这一情况在以石墨负极为主的碳材料负极出现后得到了改变,直到现在,绝大多数商业锂离子电池的负极材料依然是以石墨烯材料作为负极[2]。
从应用角度出发,负极材料的选取需要考虑多个方面,除了可逆容量、循环性能与倍率性能等,活性颗粒与导电包覆层、活性颗粒与集流体的接触性、所制备极片的压实密度、能量密度等也是不可忽略的方面,但不幸的是,在当前许多文章中往往忽视了后者。
目前,商业化的石墨材料因比容量较低(372 mAh/g)和使用过程中存在的安全隐患问题已不能满足人们对高能量密度电池组件的需求。近年来,关于负极材料的研究主要集中在碳材料、氮化物、硅基材料、锡基材料、新型合金材料、钛酸锂以及过渡金属氧化物(TMOs,M:Co,Ni,Cu,Fe,Mo)材料[3, 4]。
尽管各种高能量密度的锂电负极材料层出不穷,但始终无法解决锂离子电池当前面临的关键问题。本文将从理论层面分析并梳理负极材料当前所面临的挑战,并介绍对近年来负极材料改性研究的新思路。
负极材料所面临的挑战
实现电池的超快速充电是动力电池领域的最重要发展目标之一,超快速充电的目标是15分钟的充电时间,如果能够实现,将会大大加速电动汽车的大规模市场应用,进而为世界各国提供更强的能源保障。在超高速充电时,正极材料的容量会大幅下降,但这并不是主要问题。在负极方面,负极表面析锂是制约快速充电的主要原因[5],并且不仅仅石墨负极,嵌锂电位比较低的负极都会面临这一关键问题。
从负极材料嵌脱Li+的机理来看,以石墨负极为例,电池充电时,来自正极的Li+会通过电解质来到负极表面,随后嵌入石墨材料内,这一过程的动力是正负极之间电势差。当充电速率超过一临界值时,即电流足够大时,同时抵达负极表面的Li+数量足够多。电荷转移过电位、欧姆极化和浓度极化会使阳极电位低于Li+/Li0平衡电位当充电速率超过石墨晶体结构的插入速率时,就会发生析锂现象,也称为镀锂,此时负极会出现锂金属。金属锂的析出会造成几乎不可逆的严重后果,首先,金属锂会导致电解质的分解,这比较容易理解,活泼的金属锂很容易与电解质中的盐溶液发生一系列副反应。第二,会造成锂的损失,析出的锂可能会脱离负极材料,这部分金属锂就称为“死锂”,会造成电池容量的不可逆损失。第三,析锂可能会造成材料的内部微观缺陷[6]。
不论是研究快速充电还是提高电池的性能,研究分析负极材料的嵌锂机制是很有必要的。有几篇文章研究分析了负极材料的充电嵌锂机理,主要是针对石墨负极材料的[7-10]。在普遍认可的的机理中,石墨阳极的电荷转移,定义为Li+和e-相遇的过程,如图1所示。
① Li+在SEI/电解质界面处脱溶;
② 裸露的Li+扩散通过SEI膜;
③ 在阳极/SEI界面上发生电子的接收(来自集流体的电子),在晶体内发生锂原子的固相扩散。
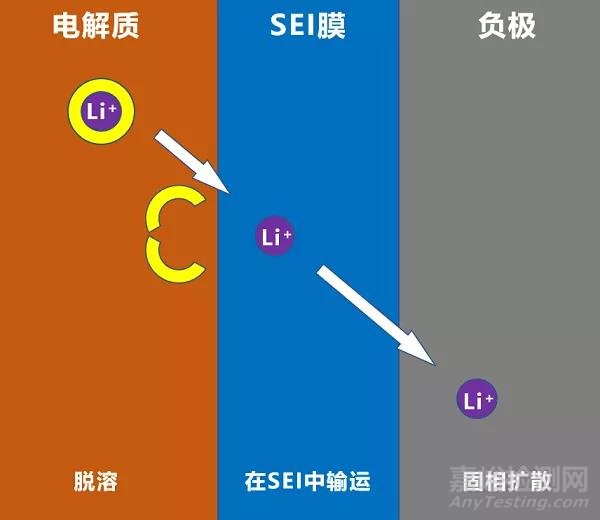
图1 负极电极过程示意
可见负极的嵌锂过程可分为三步,但是电极过程中的控制步骤是“Li脱溶”还是“Li扩散”,直到目前还没有一个定论。不可否认这三个步骤在影响电池性能方面都很重要,值得深入分析。
一些文献认为Li+脱溶步骤决定了电荷转移动力学[8, 9]。主要原因是鉴于其很小的离子半径,Li+对溶剂分子施加了很大的库仑吸引力,这阻止了脱溶过程。脱溶过程的活化能为50~60 kJ/mol。当前针对不同电解质体系中的脱溶动力学仍存在较大的研究空白,但近期一项研究中提出一个新想法[5]:以电解液添加剂或负极表面涂层引入电荷离域物质,这种物质类似于磷酸铁锂的导电聚合物包覆材料,其中存在离域的电子,能在电解质中削弱Li+与溶剂的相互作用,避免Li+被困在溶解鞘中导致脱溶活化能高,类似于竞争性溶剂化,协助Li+从溶剂分子中解离。
针对SEI,全称为Solid Electrolyte Interphase,直译为固态电解质界面,它是在液态锂离子电池首次充放电过程中,电极材料与电解液在固液相界面上发生反应,形成一层覆盖于电极材料表面的钝化层[10]。这种钝化层是一种界面层,具有固态电解质的特征,电子绝缘却是Li+的优良导体。
正极也有一层膜形成,只是现阶段认为其对电池的影响远远小于负极表面的SEI膜。负极材料石墨与电解液界面上通过界面反应能生成SEI,多种分析方法也证明SEI膜确实存在,厚度约为100~120 nm,其组成主要有各种无机成分如Li2CO3、LiF、Li2O、LiOH 等和各种有机成分如ROCO2Li、ROLi、(ROCO2Li)2等[11]。
负极的电极过程第三步骤是在负极的内部完成,即电子和离子的传输。石墨烯是一种层状材料,具有高度各向异性的固态锂扩散率。虽然他的扩散速度很快,但是这只是在平行于碳层方向的,在基面上的扩散速度可以慢4~5个数量级,这显然是限制了锂的插层动力学[12]。针对这一问题,Billaud[13]在电极制备过程中提出了一个解决方法,他提出在制备电极时降低离子路径的弯曲度,这可以加速Li+在多孔电极上的扩散输运。具体的方法是通过在电极制作过程中施加磁场,使涂有超顺磁性纳米颗粒(Fe3O4)的石墨薄片垂直于集流体。这里黑色的圆片就是石墨负极,表面涂有顺磁性颗粒,在磁场环境中涂覆与集流体上,也就是图中褐色位置(一般是铜箔),这时候石墨负极基本上取向都垂直于负极与电解质的接触面,因此很大程度上避免了Li+在石墨烯层与层之间的传递。对正极材料也有这种研究,但研究对象是钴酸锂[14, 15],关于磷酸铁锂的文献暂时没有。而磷酸铁锂材料的各向异性更加明显,Li只能在b方向传输,因此这种电极定向制备的方法在磷酸铁锂正极材料制备上或许是有价值的。
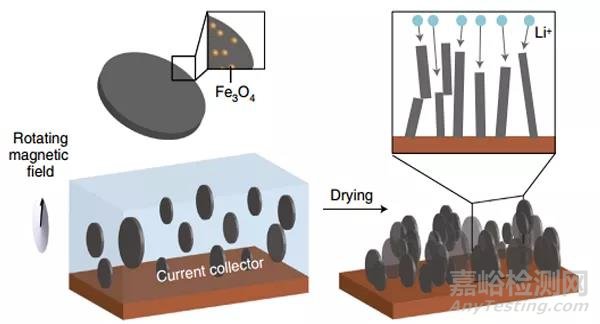
图2 磁取向负极材料示意
基于负极嵌锂机制,就可以思考在高速充电时防止负极析锂的方法。之前分析得知,析出锂金属是因为充电速率超过负极晶体结构的锂插入速率。因此可以从两个层面来避免析锂造成的危害。首先,促进负极电极过程的三个步骤,从负极材料角度来考虑,就是提高材料内的离子电导率。
从这个角度出发,我们可以借鉴磷酸铁锂纳米改性的思想:磷酸铁锂纳米化是促进离子快速传输的有效方式[16]。因此对氧化铜负极材料这种与磷酸铁锂同样离子扩散系数低的材料进行纳米化是有效的改性方法。再考虑磷酸铁锂的离子掺杂改性,主要是利用不同价位的离子在晶体中产生缺陷[17],这或许也可以用于氧化铜负极材料的改性,但目前尚无相关研究报告。
另一方面,如果产生了析锂现象,如何去避免其所造成的危害,目前在氧化铜负极材料领域的相关研究暂时处于空白,但我找到了一篇文献中提到的“种子阴极”的设计思路:金、银、锌等金属对锂有一定的溶解度,在这些金属基体上锂的成核能垒很低[18],因此如果将金纳米颗粒或银纳米颗粒嵌入石墨负极中,如果析锂现象发生,将优先在石墨内部的金颗粒处发生,因此就能将析出的锂限制在负极内,从而降低了与电解质反应和引起电池短路的风险[19]。
总结
人们已通过各种方法对负极材料进行纳米化、特殊形貌控制以及材料复合等方面的改性研究,缩短了锂离子的脱嵌路径,增大了材料与电解液的有效接触面积,抑制了材料相互之间的团聚,增强了材料的导电性。这些新颖的改性思路有效提升了材料的电化学性能,但距离其真正商业化应用尚存在一定距离。除非开发出兼具经济性与规模化制备能力的改性负极材料,否则未来很长一段时间内主流锂电负极材料将仍以石墨为主。
参考文献
[1] Zhang R, Li N, Cheng X, et al. Advanced Micro/Nanostructures for Lithium Metal Anodes[J]. Advanced Science. 2017, 4(3).
[2] Yoo E, Kim J, Hosono E, et al. Large reversible Li storage of graphene nanosheet families for use in rechargeable lithium ion batteries[J]. NANO LETTERS. 2008, 8(8): 2277-2282.
[3] Zheng M, Tang H, Li L, et al. Hierarchically Nanostructured Transition Metal Oxides for Lithium-Ion Batteries[J]. ADVANCED SCIENCE. 2018, 5(17005923).
[4] Gao X P, Bao J L, Pan G L, et al. Preparation and Electrochemical Performance of Polycrystalline and Single Crystalline CuO Nanorods as Anode Materials for Li Ion Battery[J]. The Journal of Physical Chemistry B. 2004, 108(18): 5547-5551.
[5] Liu Y, Zhu Y, Cui Y. Challenges and opportunities towards fast-charging battery materials[J]. NATURE ENERGY. 2019, 4(7): 540-550.
[6] Ishikawa K, Ito Y, Harada S, et al. Crystal Orientation Dependence of Precipitate Structure of Electrodeposited Li Metal on Cu Current Collectors[J]. CRYSTAL GROWTH & DESIGN. 2017, 17(5): 2379-2385.
[7] Xu K, von Cresce A, Lee U. Differentiating Contributions to "Ion Transfer" Barrier from Interphasial Resistance and Li+ Desolvation at Electrolyte/Graphite Interface[J]. LANGMUIR. 2010, 26(13): 11538-11543.
[8] Jow T R, Delp S A, Allen J L, et al. Factors Limiting Li+ Charge Transfer Kinetics in Li-Ion Batteries[J]. JOURNAL OF THE ELECTROCHEMICAL SOCIETY. 2018, 165(2): A361-A367.
[9] Abe T, Sagane F, Ohtsuka M, et al. Lithium-ion transfer at the interface between lithium-ion conductive ceramic electrolyte and liquid electrolyte - A key to enhancing the rate capability of lithium-ion batteries[J]. JOURNAL OF THE ELECTROCHEMICAL SOCIETY. 2005, 152(11): A2151-A2154.
[10] Peled E, Menkin S. Review-SEI: Past, Present and Future[J]. JOURNAL OF THE ELECTROCHEMICAL SOCIETY. 2017, 164(7): A1703-A1719.
[11] Verma P, Maire P, Novak P. A review of the features and analyses of the solid electrolyte interphase in Li-ion batteries[J]. ELECTROCHIMICA ACTA. 2010, 55(22): 6332-6341.
[12] Persson K, Sethuraman V A, Hardwick L J, et al. Lithium Diffusion in Graphitic Carbon[J]. JOURNAL OF PHYSICAL CHEMISTRY LETTERS. 2010, 1(8): 1176-1180.
[13] Billaud J, Bouville F, Magrini T, et al. Magnetically aligned graphite electrodes for high-rate performance Li-ion batteries[J]. NATURE ENERGY. 2016, 1(16097).
[14] Bae C, Erdonmez C K, Halloran J W, et al. Design of Battery Electrodes with Dual-Scale Porosity to Minimize Tortuosity and Maximize Performance[J]. ADVANCED MATERIALS. 2013, 25(9): 1254-1258.
[15] Sander J S, Erb R M, Li L, et al. High-performance battery electrodes via magnetic templating[J]. NATURE ENERGY. 2016, 1(16099).
[16] Chang Y, Peng C, Hung I. Effects of particle size and carbon coating on electrochemical properties of LiFePO4/C prepared by hydrothermal method[J]. JOURNAL OF MATERIALS SCIENCE. 2014, 49(20): 6907-6916.
[17] Tian Z, Zhou Z, Liu S, et al. Enhanced properties of olivine LiFePO4/graphene co-doped with Nb5+ and Ti4+ by a sol–gel method[J]. Solid State Ionics. 2015, 278: 186-191.
[18] Yan K, Lu Z, Lee H, et al. Selective deposition and stable encapsulation of lithium through heterogeneous seeded growth[J]. NATURE ENERGY. 2016, 1(16010).
[19] Sun Y, Zheng G, Seh Z W, et al. Graphite-Encapsulated Li-Metal Hybrid Anodes for High-Capacity Li Batteries[J]. CHEM. 2016, 1(2).

来源:材料人


